蓄能“创新力” 细胞技术研发与应用的突破与前景

细胞技术,作为生命科学领域的核心驱动力之一,正以前所未有的速度重塑医疗健康、生物制造乃至人类对生命本质的认知。从基础研究到临床转化,从实验室探索到产业化布局,其发展脉络清晰展现了“创新力”的持续蓄能与释放过程。本文将深入探讨细胞技术研发的关键进展、应用领域的多维拓展以及未来所面临的机遇与挑战。
一、 研发基石:从认知到操纵的跨越
细胞技术研发的“创新力”首先源于对生命基本单元——细胞——的深刻理解与精准操控能力的飞跃。
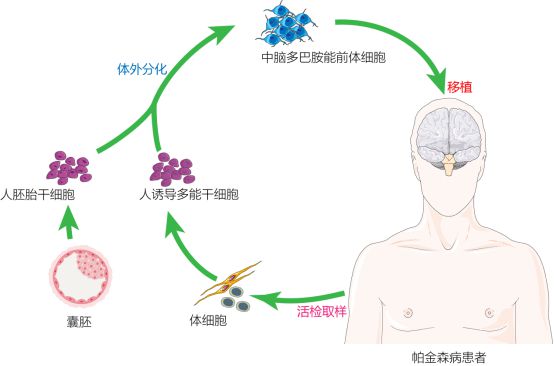
- 干细胞技术的突破: 诱导多能干细胞(iPSC)技术的成熟,实现了将体细胞“重编程”为具有多向分化潜能的干细胞,这不仅绕开了胚胎干细胞的伦理争议,更为疾病建模、药物筛选和个性化细胞治疗提供了近乎无限的细胞来源。干细胞在定向分化效率、规模培养工艺及安全性评估方面的持续优化,为其临床应用奠定了坚实基础。
- 基因编辑工具的革新: CRISPR-Cas9等基因编辑技术的出现与迭代,实现了对细胞基因组进行高效、精准的“修剪”与“改写”。这使治愈由单基因缺陷引起的疾病(如地中海贫血、镰状细胞病)成为可能,并通过编辑免疫细胞(如CAR-T细胞)来对抗癌症,开创了肿瘤免疫治疗的新纪元。新型编辑工具如碱基编辑、先导编辑的发展,进一步提升了编辑的精确度和适用范围。
- 合成生物学的融合: 将工程学原理应用于细胞,设计并构建具有新功能的“活体机器”。例如,改造微生物细胞生产高价值药物、生物燃料或可降解材料;设计免疫细胞使其具备更敏锐的肿瘤识别与杀伤能力。这标志着细胞技术从“利用”自然细胞向“设计创造”功能化细胞的范式转变。
二、 应用蓝图:多领域赋能与转化
蓄积的研发“创新力”正迅速转化为解决实际问题的应用动能,其影响辐射至多个关键领域。
- 革命性医疗(再生医学与精准治疗):
- 细胞治疗: CAR-T、TCR-T等免疫细胞疗法已在血液肿瘤治疗中取得显著成效,实体瘤攻克是当前主攻方向。干细胞移植用于修复受损组织(如心肌、神经、骨关节),治疗帕金森病、糖尿病并发症等的研究进入临床阶段。
- 组织工程与器官再造: 利用细胞、支架材料和信号因子,在体外构建或诱导体内再生功能性组织(皮肤、软骨等)。“类器官”技术能在培养皿中模拟微型器官,用于疾病研究、药物毒性与疗效测试,部分已开始替代动物实验。
- 个性化药物研发: 利用患者来源的细胞(尤其是iPSC分化细胞)建立疾病模型,加速靶点发现与药物筛选,实现“在患者身上试药前,先在其细胞模型上试药”。
- 生物制造与产业升级:
- 细胞工厂: 利用改造后的细菌、酵母或哺乳动物细胞,规模化生产传统化学合成困难或成本高昂的产物,如抗体药物、疫苗、酶制剂、香料和营养品。
- 培养肉与农业创新: 通过动物肌肉干细胞体外培养生产肉类,有望应对传统畜牧业带来的资源环境压力,并保障食品安全。植物细胞培养也可用于生产稀有次生代谢产物。
- 科学研究与生命认知: 作为基础研究的强大工具,细胞技术助力科学家解析发育生物学、疾病机制、衰老过程等根本性科学问题,不断拓展人类对生命奥秘的探索边界。
三、 未来展望:持续蓄能,应对挑战
尽管前景广阔,细胞技术的全面发展仍需持续蓄能“创新力”,并审慎应对伴随而来的挑战。
- 技术创新方向: 未来研发将更聚焦于提升技术的 安全性(如基因编辑的脱靶效应控制、干细胞治疗的成瘤风险)、有效性(如实体瘤中免疫细胞的浸润与持久性)、可控性(如细胞活性的精准调控)和 可及性(如降低CAR-T等疗法的高昂成本,开发“通用型”细胞产品)。人工智能与大数据分析在细胞设计、培养过程优化和疗效预测中的应用将日益深入。
- 产业化与监管挑战: 细胞产品(尤其是活细胞)的规模化、标准化、自动化生产与质控体系亟待完善。与之相适应的、既鼓励创新又确保安全有效的动态监管框架是全球监管机构面临的共同课题。
- 伦理与社会考量: 基因编辑生殖细胞(可遗传编辑)引发的伦理争议巨大,国际社会对此持高度谨慎态度。细胞技术的公平可及性、个人信息与遗传数据保护、公众认知与接受度等问题也需要同步关注与引导。
###
蓄能“创新力”是细胞技术发展的永恒主题。从微观的基因剪接,到宏观的产业变革,细胞技术正将一个个科幻般的构想变为现实。只有坚持基础研究的原始创新,推动跨学科的深度融合,构建健全的产业生态与伦理法规体系,才能确保这股强大的“创新力”得到负责任且高效的应用,最终为人类健康、经济可持续发展和社会进步注入源源不断的生机与活力。
如若转载,请注明出处:http://www.nicellsmall.com/product/18.html
更新时间:2026-03-07 17:14:29